Degarelix, som säljs under varumärket Firmagon, är en pivotal hormonbehandling vid behandling av prostatacancer. Som en syntetisk peptid och en potent Gonadotropin-Releasing Hormone (GnRH)-receptorantagonist, är dess primära och mest väletablerade användning för androgendeprivationsterapi (ADT) hos patienter med avancerad, hormonkänslig prostatacancer. Till skillnad från traditionella GnRH-agonister,Degarelix erbjuder en unik verkningsmekanism som ger snabb och ihållande testosteronundertryckning utan en initial tumörstimulerande flare, vilket gör det till ett kritiskt behandlingsalternativ för specifika patientpopulationer. Den här artikeln utforskar dess kärnindikationer, mekanism, klinisk effekt, säkerhetsprofil och nya tillämpningar, med stöd av auktoritativa kliniska data och regulatoriska riktlinjer.
Verkningsmekanism: Direkt och snabb hormondämpning
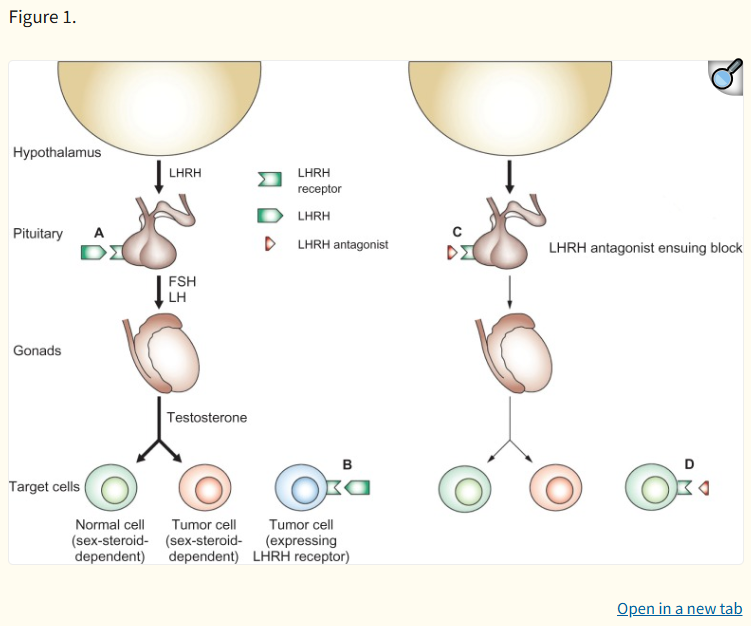
Den terapeutiska kraften avDegarelix härrör från dess direkta kompetitiva blockad av GnRH-receptorer i hypofysen. Hypothalamus frisätter naturligt GnRH för att stimulera hypofysen att utsöndra luteiniserande hormon (LH) och follikelstimulerande hormon (FSH). Dessa hormoner signalerar sedan testiklarna att producera testosteron, en nyckelfaktor för tillväxt av prostatacancerceller.
Degarelix binder tätt och reversibelt till dessa hypofysreceptorer, vilket omedelbart stoppar frisättningen av LH och FSH. Denna snabba hämning leder till en dramatisk och snabb minskning av produktionen av testikeltestosteron. En avgörande fördel jämfört med GnRH-agonister är frånvaron av en initial "testosteronökning" eller klinisk flare. Agonister överstimulerar initialt receptorerna, vilket orsakar en övergående ökning av testosteron som kan förvärra symtom som skelettsmärta eller urinvägsobstruktion hos sårbara patienter.Degarelix undviker denna farliga fas, börjar testosteronundertryckning den första dagen av administreringen och uppnår medicinska kastrationsnivåer (≤0,5 ng/ml eller 50 ng/dL) hos över 96 % av patienterna på dag 3. Denna snabba debut är avgörande för patienter som behöver omedelbar sjukdomskontroll.

Primärt godkända indikationer: Avancerad och högrisk prostatacancer
Degarelix är globalt godkänt, inklusive av U.S. FDA och European Medicines Agency (EMA), specifikt för behandling avavancerad, hormonberoende prostatacancer. Dess kliniska profil gör den särskilt lämpad för flera nyckelscenarier inom denna breda indikation:
Avancerad prostatacancer (metastaserande eller lokalt avancerad): Detta är FDA-godkänd kärnanvändning. Det är indicerat för patienter med metastaserande sjukdom, där cancer har spridit sig utanför prostata, eller lokalt avancerad sjukdom (T3/T4), där den har spridit sig utanför prostata men inte till avlägsna organ. Målet är att inducera och upprätthålla långvarig testosteronundertryckning för att bromsa eller stoppa cancertillväxt.
Lokaliserad prostatacancer med hög risk (i kombination med strålbehandling): EMA och kliniska riktlinjer godkännerDegarelix som en del av en kombinerad metod. För patienter med högrisk lokaliserad eller lokalt avancerad prostatacancer används den som neoadjuvant (förbehandling) och samtidigt behandling med strålbehandling. Denna kombination förbättrar lokal kontroll och överlevnad genom att krympa tumören före strålning och undertrycka hormondriven tillväxt under behandlingen.
Patienter som löper risk för flare symtom: På grund av sin brist på initial testosteronökning,Degarelix är det föredragna ADT-valet för patienter med symtomatiska metastaser, förestående ryggmärgskompression, allvarlig urinvägsobstruktion eller de med hög kardiovaskulär risk. Dessa patienter kan inte tolerera den potentiella symtomexacerbationen orsakad av GnRH-agonister.
Andra linjens terapi eller för patienter som är intoleranta mot agonister: Det fungerar som ett effektivt alternativ för patienter som har utvecklats eller inte kan tolerera biverkningarna av vanliga GnRH-agonistterapier.

Klinisk effekt: Beprövad prestanda i nyckelstudier
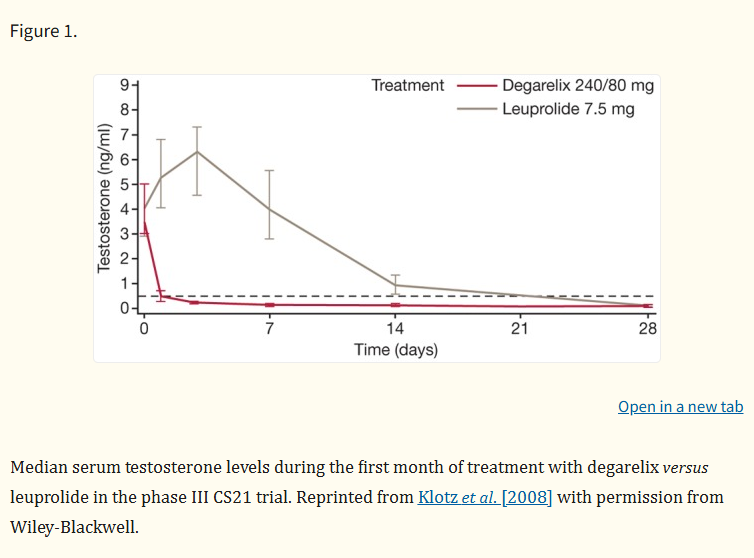
Effekten avDegarelix har rigoröst etablerats i kliniska fas III-prövningar, framför allt en stor, randomiserad, öppen studie som jämför den med GnRH-agonisten leuprolid hos över 600 prostatacancerpatienter.
Det primära effektmåttet var att bibehålla testosteron på kastratnivåer i ett år. Resultaten visade detDegarelix (vid både 80 mg och 160 mg underhållsdoser) var icke-sämre än leuprolid, med över 97 % av patienterna som uppnådde ihållande suppression. Rättegångens mest slående fynd var undertryckningens hastighet: på dag 3, 96,5 % avDegarelix patienterna kastrerades, jämfört med 0 % i leuprolidgruppen. Denna snabba kontroll åtföljdes av en betydligt snabbare minskning av nivåerna av prostataspecifikt antigen (PSA), en viktig biomarkör för sjukdomsaktivitet.
En omfattande metaanalys bekräftade dessa fynd, vilket ytterligare belyser detDegarelix ger överlägsen lindring av symtom i de nedre urinvägarna och är associerad med en lägre risk för kardiovaskulära biverkningar jämfört med agonister. Dess effektivitet bibehålls med månatliga subkutana injektioner, vilket bildar en bekväm och effektiv långtidsbehandling.
Säkerhetsprofil och administration
Degarelix administreras som en subkutan bukinjektion, med en startdos på 240 mg (två 120 mg injektioner) följt av månatliga underhållsdoser på 80 mg. Dess säkerhetsprofil är välkarakteriserad.
De vanligaste biverkningarna ärreaktioner på injektionsstället (t.ex. smärta, rodnad, svullnad), som förekommer hos cirka 40-50 % av patienterna, främst med den initiala dosen. Dessa är i allmänhet milda till måttliga och minskar med tiden. Andra frekventa biverkningar är typiska för ADT och inkluderar värmevallningar, viktförändringar, trötthet och övergående ökningar av leverenzymer (transaminaser).
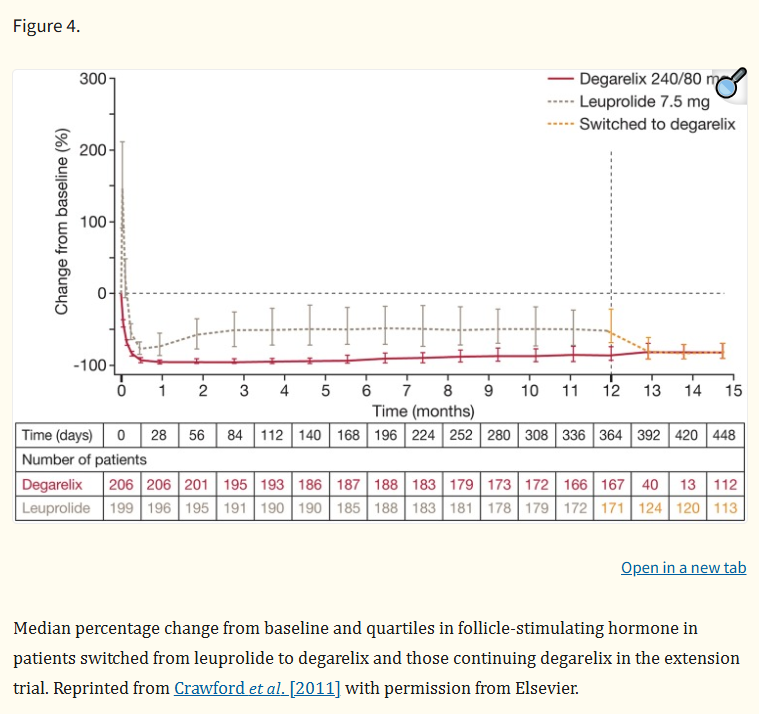
En betydande säkerhetsfördel är dess mer gynnsamma kardiovaskulära profil jämfört med GnRH-agonister. Metaanalyser visar en lägre incidens av allvarliga kardiovaskulära händelser, en kritisk faktor för äldre patienter med flera komorbiditeter. Men som med alla ADT måste vårdgivare övervaka potentiell QT-intervallförlängning, särskilt hos patienter med redan existerande hjärtsjukdomar eller på samtidig medicinering som påverkar hjärtats elektriska cykel.Degarelix är kontraindicerat hos patienter med allvarlig överkänslighet mot läkemedlet och hos kvinnor som är eller kan bli gravida.
Nya och off-label applikationer
Medan avancerad prostatacancer fortfarande är dess enda formella indikation, undersöker forskningen Degarelix potential inom andra områden. Dess potenta och snabba testosteronundertryckande undersöks förneoadjuvant terapi före radikal prostatektomi hos högriskpatienter, som syftar till att krympa tumörer och förbättra kirurgiska resultat. Preliminära studier tyder också på en potentiell roll i att hanterakastrationsresistent prostatacancer (CRPC) i kombination med nyare androgenreceptorinriktade terapier.

Det finns också begränsad forskning om dess användning för godartade tillstånd sombenign prostatahyperplasi (BPH), där minskning av testosteron kan lindra urinvägssymtom, även om detta förblir off-label och inte en standard för vård.
Slutsats
Sammanfattningsvis,Degarelix (Firmagon) är en specialiserad och mycket effektiv GnRH-antagonist, som främst används för behandling av androgenberövandeavancerad, hormonkänslig prostatacancer. Dess unika försäljningsargument är desssnabbt insättande av verkan, frånvaro av en testosteronflamma, ochgynnsam kardiovaskulär säkerhetsprofil jämfört med äldre agonistterapier. Dessa egenskaper gör det till den bästa behandlingen för patienter som behöver omedelbar sjukdomskontroll eller de som löper risk för komplikationer från en hormonökning. Uppbackad av robusta data från kliniska prövningar,Degarelix representerar ett betydande framsteg inom hormonbehandling, och erbjuder ett värdefullt och ofta föredraget alternativ för urologer som behandlar patienter över hela spektrumet av avancerad prostatacancer och högriskprostatacancer.
Posttid: 2026-04-13
