Nyckelord:NAD+,53-84-9,NAD+ bioaktiv peptid
NAD+, förkortningen av Nicotinamide Adenine Dinukleotid, är ett livsviktigt koenzym som finns i alla levande celler i människokroppen, och är också kärnmolekylen som förbinder cellmetabolism, DNA-reparation, åldrandereglering och sjukdomsförekomst. Sedan upptäckten 1904 har NAD+ bekräftats delta i mer än 500 typer av enzymatiska reaktioner i kroppen och är oumbärlig för att upprätthålla normala livsaktiviteter. Det är inte bara en nyckelelektronbärare i processen för energimetabolism, utan också ett väsentligt substrat för att aktivera viktiga proteiner som Sirtuins och PARPs, som bestämmer energitillförseln, reparationsförmågan och åldringshastigheten hos celler. Med den fördjupade forskningen har NAD+ blivit en hot spot inom områdena anti-aging, behandling av metabola sjukdomar och neuroprotection, och dess nivåförändring betraktas som en viktig biomarkör för kroppens åldrande och hälsostatus.
Den kemiska strukturen och grundläggande former av NAD+
NAD+ är en liten molekyl som består av två nukleotider, nämligen nikotinamidmononukleotid (NMN) och adenindinukleotid, och dess struktur innehåller nikotinamid (ett derivat av vitamin B3), adenin, ribos och fosfatgrupper. Det finns huvudsakligen i två interkonvertibla former i celler: oxiderad NAD+ och reducerad NADH. NAD+ är i ett "tomt" tillstånd och kan acceptera elektroner som genereras under metaboliska reaktioner, medan NADH är i ett "fullständigt" tillstånd som bär elektroner, som kan frigöra elektroner i mitokondriella andningskedjan för att främja ATP-syntes. Cykelomvandlingen mellan NAD+ och NADH (NAD+ ↔ NADH) är kärnan i cellenergiproduktion, och förhållandet mellan NAD+/NADH påverkar direkt effektiviteten av energimetabolism och redoxtillståndet hos cellerPMC. Dessutom kan NAD+ fosforyleras för att bilda NADP+, och dess reducerade form NADPH används huvudsakligen för antioxidativ stress och anabola reaktioner som kräver reducerande kraft, samtidigt som balansen mellan cellredox upprätthålls.

NAD+ är kärnan i cellulär energimetabolism
Den mest grundläggande funktionen hos NAD+ är att fungera som ett nyckelkoenzym i cellulär energimetabolism, ansvarig för överföring av elektroner i glykolys, trikarboxylsyracykel (TCA-cykel) och fettsyraoxidationsprocesser. När människokroppen smälter och absorberar kolhydrater, fetter och proteiner bryts dessa näringsämnen ner till små molekyler och kommer in i mitokondrierna. Vid denna tidpunkt accepterar NAD+ kontinuerligt vätejoner och elektroner som avlägsnas under nedbrytningsprocessen och omvandlas till NADH. NADH transporterar sedan dessa högenergielektroner till den mitokondriella elektrontransportkedjan, och genom en serie redoxreaktioner främjar slutligen syntesen av ATP, cellers direkta energivaluta. Denna process ger mer än 90 % av den energi som krävs för livsaktiviteter, och stöder grundläggande fysiologiska funktioner som hjärtslag, hjärntänkande, muskelsammandragning och celldelning. Utan tillräckligt med NAD+ kan celler inte omvandla mat till energi, och alla livsaktiviteter kommer att blockeras, vilket fullt ut återspeglar den oersättliga betydelsen av NAD+.
NAD+ dominerar DNA-reparation och genomisk stabilitet
DNA-skada är en oundviklig händelse i celllivsprocessen, och snabb reparation är nyckeln till att upprätthålla genomisk stabilitet och förhindra cellmutation och åldrande. NAD+ spelar en central roll i denna process som ett väsentligt substrat för poly (ADP-ribos) polymeras (PARP). När DNA-enkelsträngade eller dubbelsträngade brott inträffar, aktiveras PARP snabbt och förbrukar en stor mängd NAD+ för att syntetisera ADP-riboskedjor, som rekryterar och aktiverar en mängd olika DNA-reparationsproteiner för att fullborda reparationen av skadade platser. Samtidigt är NAD+ också en nödvändig kofaktor för Sirtuins-proteinfamiljen (inklusive SIRT1, SIRT3, SIRT6, etc.). Sirtuiner, kända som "livslängdsproteiner", förlitar sig på NAD+ för att utöva deacetyleringsaktivitet, reglera cellcykeln, hämma cellapoptos, förbättra cellstressresistens och ytterligare upprätthålla stabiliteten hos kromosomer och gener. Studier har bekräftat att avsaknaden av NAD+ kommer att leda till nedgången av PARP- och Sirtuins aktiviteter, vilket resulterar i ackumulering av DNA-skador, accelererar cellåldring och ökar risken för relaterade sjukdomar.

NAD+ reglerar åldrande och åldersrelaterade sjukdomar
Ett stort antal studier har bekräftat att nivån av NAD+ i olika vävnader och organ hos däggdjur minskar signifikant med åldern. Forskning från Harvard Medical School visar att efter 25 års ålder sjunker människokroppens NAD+-nivå med en hastighet av 12 % till 15 % per år; vid 40 års ålder är det bara cirka 50 % av det vid 20 års ålder; vid 60 års ålder sjunker den till 20 % till 30 %. Denna progressiva nedgång är nära relaterad till förekomsten av åldrande och åldranderelaterade sjukdomar. Låga NAD+-nivåer leder till försvagad mitokondriell funktion, minskad energiproduktion, ökad oxidativ stress och försämrad DNA-reparationskapacitet, vilket i sin tur utlöser en rad åldrande manifestationer som trötthet, minnesförlust, hudavslappning och metabola störningar. Dessutom är nedgången av NAD+ också associerad med patogenesen av många kroniska sjukdomar, inklusive typ 2-diabetes, hjärt-kärlsjukdomar, neurodegenerativa sjukdomar (Alzheimers sjukdom, Parkinsons sjukdom) och muskelatrofi. En studie publicerad i Nature Aging (2025) påpekade att återställande av NAD+-nivåer kan förbättra mitokondriell funktion, skydda neuroner och fördröja utvecklingen av åldersrelaterade sjukdomar. En annan studie i Cell Metabolism (2020) bekräftade att NAD+ prekursortillskott kan vända åldringsrelaterad muskelatrofi och förbättra fysisk uthållighet.

Biosyntesvägar och tilläggsstrategier för NAD+
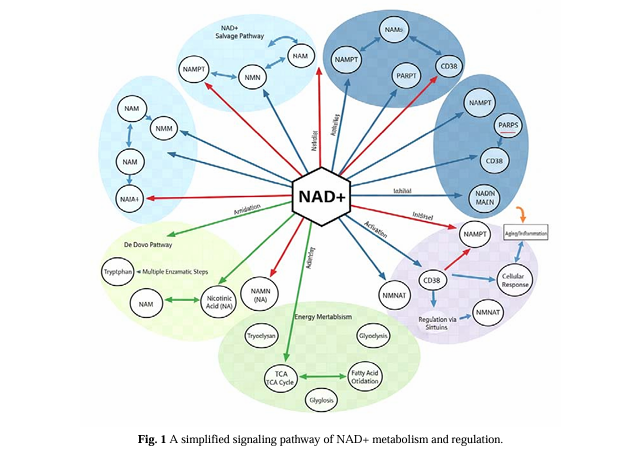
Människokroppen syntetiserar huvudsakligen NAD+ genom två vägar: de novo syntesvägen och räddningsvägenPMC. De novo syntesvägen startar från tryptofan och fullbordas genom flera enzymatiska reaktioner, med låg effektivitet PMC. Bärgningsvägen är det huvudsakliga sättet för kroppen att generera NAD+, som använder nikotinamid (NAM), nikotinamidribosid (NR), nikotinamidmononukleotid (NMN) och andra prekursorer för att syntetisera NAD+ genom en serie reaktioner, bland vilka Nicotinamide Fosforibosyltransferas (NAMP.T) är enzymet rate-PM (NAMP.T). Med åldern minskar aktiviteten av NAMPT och nedbrytningen av NAD+ (främst medierad av CD38-enzym) ökar, vilket leder till en kontinuerlig minskning av NAD+-nivåerPMC. För närvarande inkluderar de viktigaste sätten att öka NAD+-nivåerna i kroppen att komplettera NAD+-prekursorer (som NMN, NR), hämma CD38-enzymaktivitet och förbättra NAMPT-aktiviteten. Bland dem kan NMN och NR, som direkta prekursorer till NAD+, effektivt omvandlas till NAD+ efter att ha kommit in i cellerna, och har blivit de mest undersökta och tillämpade näringstillskottsingredienserna. Kliniska studier har visat att rimligt tillskott av NAD+-prekursorer effektivt kan öka kroppens NAD+-nivå, förbättra energiomsättningen, förbättra träningskapaciteten, förbättra sömnkvaliteten och lindra kognitiv försämring.
Slutsats
Sammanfattningsvis är NAD+ (Nicotinamide Adenine Dinucleotide) ett kärnkoenzym som upprätthåller livsaktiviteter, integrerar energimetabolism, DNA-reparation, åldrandereglering och sjukdomsförsvar. Det är inte bara cellernas "kraftmotor", ansvarig för att omvandla mat till energi, utan också "reparatören" av gener, som upprätthåller genomets stabilitet; det är också en "regulator" av åldrande, och dess nivåförändringar bestämmer direkt hastigheten på cellåldring och kroppens hälsostatus. Nedgången av NAD+-nivån är en viktig orsak till åldrande och kroniska sjukdomar, och att rimligt återställa NAD+-nivån har blivit en nyckelstrategi för att främja hälsosamt åldrande och förebygga relaterade sjukdomar. Med det kontinuerliga genombrottet av vetenskaplig forskning kommer NAD+ att spela en större roll inom hälsovård och klinisk medicin, vilket ger nytt hopp för människors hälsa och livslängd.
Posttid: 2026-04-16
